Luigi Ricciardi 1 , Rosa Mazzeo 2,*© , Angelo Raffaele Marcotrigiano 1 , Guglielmo Rainaldi 3 , Paolo Iovieno 4 , Vito Zonno 1 , Stefano Pavan 1© ja Concetta Lotti 2,*
- 1 Bari ülikooli mulla-, taime- ja toiduteaduste osakond, taimegeneetika ja -aretusüksus, Via Amendola 165/A, 70125 Bari, Itaalia; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (ARM); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Põllumajandus-, toidu- ja keskkonnateaduste osakond, Foggia ülikool, Via Napoli 25, 71122 Foggia, Itaalia
- 3 Bioteaduste, biotehnoloogiate ja biofarmaatsia osakond, Bari Ülikool, Via Orabona 4, 70125 Bari, Itaalia; guglielmo.rainaldi@uniba.it
- 4 Energiatehnoloogiate osakond, bioenergia, biorafineerimistehase ja rohelise keemia osakond, ENEA Trisaia Research Center, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Itaalia; paolo.iovieno@enea.it
* Kirjavahetus: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Abstraktne:
Sibul (Allium cepa L.) on maailmas tähtsuselt teine köögiviljakultuur ja seda hinnatakse laialdaselt selle kasulikkuse tõttu tervisele. Vaatamata selle olulisele majanduslikule tähtsusele ja väärtusele funktsionaalse toiduna, on sibulat selle geneetilise mitmekesisuse osas vähe uuritud. Siin uurisime Bari provintsi (Apuulia, Lõuna-Itaalia) väikelinnas sajandivanuse viljelusajalooga maatõugu „Acquaviva punase sibula” (ARO) geneetilist variatsiooni. 11 ARO populatsioonist ja kolmest tavalisest kaubanduslikust tüübist koosneva iduplasma kollektsiooni geneetilise variatsiooni uurimiseks kasutati 13 mikrosatelliidi markeri komplekti. Geneetilise struktuuri analüüsid parameetriliste ja mitteparameetriliste meetoditega tõid esile, et ARO esindab täpselt määratletud geenifondi, mis erineb selgelt Tropea ja Montoro maatõugudest, millega seda sageli eksitakse. Tavaliselt värskeks tarbimiseks kasutatavate sibulate kirjeldamiseks hinnati lahustuva tahke aine sisaldust ja teravust, mis näitas ARO-s kõrgemat magusust võrreldes kahe eespool nimetatud maatõuga. Üldiselt on käesolev uuring kasulik ARO tulevaseks väärtustamiseks, mida saaks edendada kvaliteedimärgiste abil, mis võiksid aidata piirata kommertspettusi ja parandada väiketalunike sissetulekuid.
Sissejuhatus
Perekonda Allium kuulub umbes 750 liiki [1], mille hulgas on sibul (Allium cepa L., 2n = 2x =16) üks levinumaid. A. cepal on kaheaastane tsükkel ja ristuva paljunemiskäitumine. Sibula ülemaailmne toodang (97.9 Mt) teeb sellest tänapäeval tomati järel tähtsuselt teise köögiviljakultuuri [2]. Sibulasibulaid on iidsetest aegadest kasutatud nii toiduna kui ka rahvameditsiinis. Tõepoolest, iidsed egiptlased teatasid juba mitmest terapeutilisest valemist, mis põhinesid küüslaugu ja sibula kasutamisel 1550 eKr meditsiinilises papüüruses Codex Ebers [3].
Seda mitmekülgset ja tervislikku köögivilja tarbitakse toorelt, värskelt või töödeldud tootena ning seda kasutatakse paljude roogade maitse parandamiseks. Mitmed hiljutised uuringud väidavad, et sibula tarbimine võib vähendada südame-veresoonkonna haiguste [4,5], rasvumise [6], diabeedi [7] ja erinevate vähivormide [8–10] riski. Sibula terviseomadused on sageli omistatud kahe klassi toitaineühendite kõrgele sisaldusele: flavonoidid ja alk(en)üültsüsteiinsulfoksiidid (ACSO-d). Esimesse klassi kuuluvad flavonoolid ja antotsüaanid. Kvertsetiin on peamine tuvastatav flavonool, mis on tuntud oma tugevate antioksüdantsete ja põletikuvastaste omaduste poolest vabade radikaalide püüdmisel ja siirdemetallide ioonide sidumisel. [11]; samas kui antotsüaniinid annavad mõnele sibulasordile punase/lilla värvuse. ACSO-de osas on kõige rohkem isoalliin [(+)-trans-S-1-propenüül-L-tsüsteiinsulfoksiid] [12], rakkudesse talletatud mittelenduv ja mitteproteinogeenne väävli aminohape, mis vastutab kaudselt sibula terava aroomi ja maitse eest [13]. Kudede katkestamisel lõhustatakse isoalliin ensüümi alliinaasi toimel, et tekiks rida lenduvaid ühendeid (püruvaat, ammoniaak, tiosulfonaadid ja propanetiaalne S-oksiid), mis kutsuvad esile pisaravoolu ja põhjustavad ebameeldivat lõhna (teravus). [14]. Sibula teravust mõõdetakse sageli hüdrolüüsil tekkinud püroviinamarihappe kogusena värske massi grammi kohta. [15, 16].
Vahemere piirkonna riikides pakuti seda üheks teiseseks mitmekesisuse keskuseks A. cepa [17, 18], sibula sibulate kuju, suurus, värvus, kuivaine ja teravus on väga erinevad [19-üks]. Veelgi enam, väävlipõhine väetamine, agronoomilised tavad, pinnase tüüp, kliimatingimused ja kultivaride või maatõugude genotüüp võivad sibulate kvaliteeti mõjutada, andes omapärased organoleptilised ja toiteväärtused. [23-üks]. Vaatamata sibula iduplasma laialdasele kättesaadavusele tehakse Itaalias sageli teaduslikke uuringuid ja iseloomustatakse neid õigesti vaid mõne sibulasordiga. [28, 29].
Põllumajandusliku bioloogilise mitmekesisuse põhjalik geneetiline ja fenotüübiline iseloomustus on ülioluline, et tagada taimede geneetiliste ressursside asjakohane säilimine ja edendada konkreetsete genotüüpide kasutamist väärtusahelas. [30-üks]. Sageli on kaardistamiseks valitud lihtsad järjestuse kordusmarkerid (SSR). [33-üks], DNA sõrmejälgede võtmine ja kultivaride diskrimineerimine [36-üks]ja geneetilise varieeruvuse usaldusväärne hindamine maatõugude sees ja nende vahel [39-üks], kuna need on lookusespetsiifilised, multialleelsed, kodominantselt päritud, hästi reprodutseeritavad ja sobivad automaatseks genotüpiseerimiseks.
Käesolevas uuringus keskendusime Apuulia traditsioonilisele maatõule, Acquaviva punasele sibulale (ARO), mida kasvatatakse mahepõllumajandusmeetodite kohaselt väikesel alal Acquaviva delle Fonti linnas Bari provintsis. (Apuulia, Lõuna-Itaalia). Selle maatõu sibulad on suured, lamedad ja punase värvusega ning neid kasutatakse suures osas kohalikes retseptides. Kuigi ARO sai kvaliteedimärgi "Slow Food Presidium", võiks selle tootmist veelgi edendada ja kaitsta Euroopa Liidu kvaliteedimärkidega, nagu kaitstud geograafiline tähis (KGT) ja kaitstud päritolunimetus (POD), kuna need võivad aidata piirata kommertspettusi ja parandada väiketalunike sissetulekuid. Siin kasutati SSR molekulaarseid markereid võimsate vahenditena ARO populatsioonide geneetilise varieeruvuse hindamiseks ja selle maatõu eristamiseks kahest teisest Lõuna-Itaalia punase sibula maatõust. Lisaks hindasime teravust ja lahustuva tahke aine sisaldust, et hinnata ARO maitset seoses turunõudlusega.
Tulemused
Acquaviva punase sibula iduplasma kogumise ja morfoloogilise iseloomustuse loomine
ARO iduplasma kollektsiooni loomiseks kasutati 13 ARO maatõu populatsiooni seemneid, mille põllumehed annetasid BiodiverSO Apuulia piirkonna projekti raames.
Morfoloogilised deskriptorid, mis on seotud sibula, naha ja viljalihaga, koguti ARO iduplasma ja kolme sibula maatõu kohta, millest kaks kuulusid Tropea punase sibula (TRO) ja üks Montoro vasksibula (MCO) maatõu (joonis joonis). 1). Kõik ARO pirnid olid lamedad ja neid iseloomustas punane väliskest ja viljaliha, millel olid erinevad punased toonid. Seevastu TRO-sibulate viljaliha oli täielikult punane, samas kui MCO-sibulate viljaliha oli halvasti pigmenteeritud (tabel S1). Biokeemiline analüüs võimaldas hinnata tahke aine sisaldust ja teravust. Nagu on näidatud tabelis 1, Sibulate tahke lahustuva sisalduse keskmised väärtused ARO populatsioonides olid 7.60 ja jäid vahemikku 6.00 (ARO12) kuni 9.50° Brixi (ARO11 ja ARO13). See väärtus oli kõrgem kui TRO ja MCO maatõugude hinnanguline väärtus (vastavalt 4.25 ja 6.00 ° Brix).

Tabel 1. Acquaviva punase sibula (ARO), Tropea punase sibula (TRO) ja Montoro vasksibula (MCO) populatsioonides hinnatud tahkete lahustuvate ainete sisalduse ja teravuse väärtused *.
| KOOD | Lahustuv tahke sisaldus (Brix) | Teravus (pmolg-1 FW) | ||
| Keskmine | CV y (%) | Keskmine | CV y (%) | |
| ARO1 | 6.25 D* | 5.65 | 5.84 ab * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 | 22.98 |
| ARO3 | 7.50 XNUMX XNUMX BCD | 9.42 | 5.28 ab | 22.88 |
| ARO4 | 7.50 XNUMX XNUMX BCD | 0.00 | 6.97 | 3.74 |
| ARO 5 | 7.50 XNUMX XNUMX BCD | 0.00 | 6.80 | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 ab | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 ab | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 ab | 6.57 |
| ARO11 | 9.50 | 7.44 | 5.54 ab | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 ab | 9.70 |
| ARO13 | 9.50 | 7.44 | 6.63 | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 ab | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 b | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 ab | 4.79 |
* Samade suur- või väiketähtedega vahendid ei erine statistiliselt vastavalt 0.01P või 0.05P juures (SNK test). y Variatsioonikoefitsient.
ARO teravuse keskmine väärtus, mida hinnati püroviinamarihappe sisalduse järgi, oli 6.00, vahemikus 4.51 pmol g-1 FW (ARO6) kuni 7.04 (ARO8). See väärtus oli kõrgem kui TRO ja MCO maatõugude puhul hinnatud väärtus (3.54 pmol g-1 FW ja 4.18 pmol g-1 vastavalt FW).
SSR polümorfism ja geneetilised suhted liitumiste vahel
Käesolevas uuringus andis 11 testitud SSR-i praimerite kombinatsioonist 37 ühe lookuse polümorfisme, st andsid maksimaalselt kaks amplifikatsiooniprodukti ühes indiviidis. Üldiselt tuvastati 55 isikul 320 alleeli, mille alleelide arv lookuse kohta oli vahemikus 2 (ACM147 ja ACM 504) kuni 11 (ACM132) ja keskmine väärtus 5 alleeli (tabel 2). Üksikutes populatsioonides jäi alleelide (Na) arv vahemikku 1.94 (ACM147 ja ACM504) kuni 5.38 (ACM132), samas kui efektiivne alleelide arv (Ne) oli vahemikus 1.41 (ACM152) kuni 2.82 (ACM449). Lahknevused Na ja Ne väärtuste vahel olid tingitud madala sagedusega alleelide olemasolust populatsioonides ja vaid mõne alleeli ülekaalust. Suurim täheldatud heterosügootsuse (Ho) väärtus tõsteti esile ACM138 ja ACM449 puhul (0.62, 152), samas kui madalaim oli seotud ACM0.25 (0.37, 504). Eeldatav heterosügootsus (He), mis vastab teoreetilisele ootusele panmiktilise populatsiooni puhul, oli vahemikus 0.61 (ACM132) kuni 138 (ACM449, ACM0.05 ja ACM0.48). Wrighti fikseerimisindeks (Fis) kuvas kõigi markerite nullilähedased väärtused (keskmiselt 0.33, 504), mis näitab sarnaseid väärtusi täheldatud ja eeldatava heterosügootsuse taseme vahel, nagu eeldati ristamise liikide puhul. Individuaalse SSR-markeri efektiivsust geneetilisel sõrmejälgede võtmisel hinnati polümorfse teabesisalduse (PIC) indeksi abil, mille keskmine väärtus oli 0.67, 132 ja oli vahemikus 0.84, 0.45 (ACM152) kuni 1.20, 132 (ACMXNUMX). Teine tõhususe indeks, Shannoni teabeindeks (I) näitas keskmist väärtust XNUMX ja eeldatavad väärtused jäid vahemikku XNUMX (ACMXNUMX) kuni XNUMX (ACMXNUMX).
Tabel 2. ARO, TRO ja MCO populatsioonide geneetilise mitmekesisuse hindamiseks kasutatud 11 SSR-markeri polümorfismi tunnused. Alleelide koguarv (Na), riba suurusvahemik ja polümorfse teabe sisu (PIC) indeks Vt selles uuringus genotüüpitud 320 indiviidi kogukomplekti. Alleelide arv (Na), efektiivsete alleelide arv (Ne), täheldatud heterosügootsus (Ho), eeldatav heterosügootsus (He), fikseerimisindeks (F)is) ja Shannoni teabeindeks (I) viitavad keskmistele väärtustele, mis on arvutatud 16 populatsiooni põhjal, millest igaüks koosneb 20 indiviidist.
| Locus. | Kokku Na | Suuruse vahemik (bp) | PIC | Keskmine | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Keskmine | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Populatsioonide hulgas oli ARO3, ARO6, ARO8, ARO10, TRO1 ja MCO kõrge geneetilise variatsiooni tase (Ho> 0.5, 7), samas kui väikseimat mitmekesisust täheldati populatsioonis ARO0.27 (Ho = 2, XNUMX) (täiendav tabel SXNUMX). Üldiselt näitasid kõik liitumised Fis nullilähedased väärtused (Fis keskmine väärtus = 0.054), nagu eeldati juhuslikes paaritumistingimustes.
Molekulaarse dispersiooni ja geneetilise struktuuri analüüs
Geneetilise variatsiooni hierarhilise jaotuse populatsioonide vahel ja sees arvutas AMOVA. Tulemused tõid esile märkimisväärse osa populatsioonide geneetilisest variatsioonist (87%). Erinevus populatsioonide vahel, 13%, oli väga oluline (P < 0.001) (Tabel 3). Wrighti Fst fikseerimisindeksi analoogi Fpt parameetri paarilised väärtused vahemikus 0.002 (ARO2/ARO10) kuni 0.468 (ARO7/TRO2) olid olulised (P < 0.05, 3), välja arvatud üheksa paaripõhist võrdlust (täiendav tabel SXNUMX).
Tabel 3. 320 genotüübi molekulaarse dispersiooni analüüs 16 populatsioonist Allium cepa L.
| allikas | df | Ruutude summa | Dispersiooni hindamine | Erinevus (%) | Fpt | P |
| Populatsioonide seas | 15 | 458.63 | 1.16 | 13% | ||
| Populatsioonide sees | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Summa | 319 | 2731.62 | 8.66 |
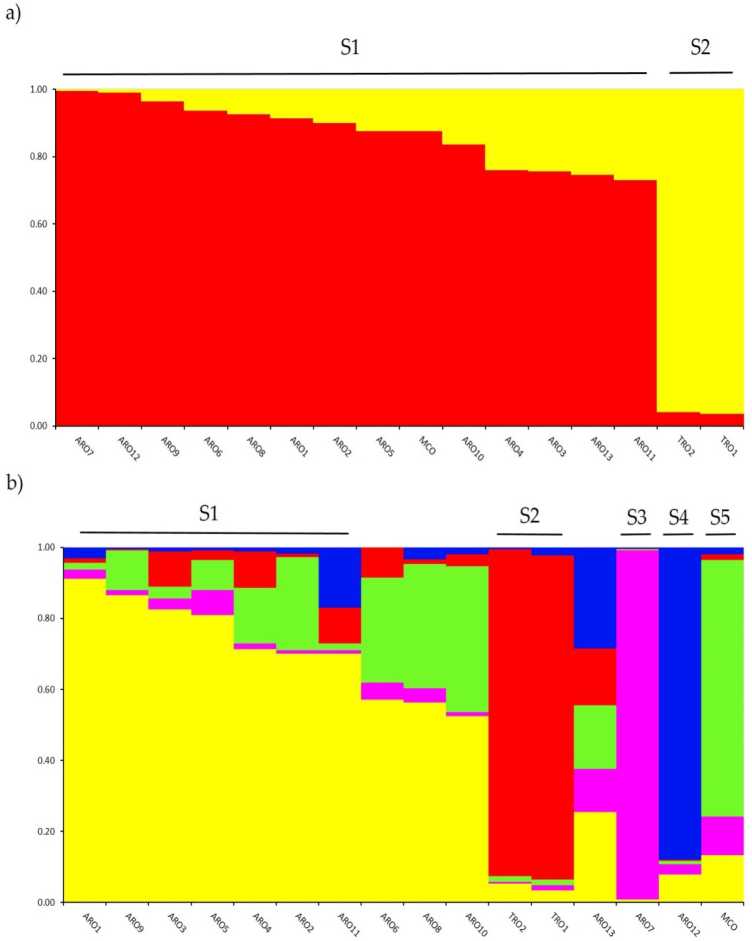
Geneetilise struktuuri uurimine A. cepa Selles uuringus genotüüpitud kollektsioon viidi läbi tarkvaras STRUCTURE rakendatud segumudelipõhise klastrianalüüsi abil. Evanno AK meetod soovitas meie jaoks kõige informatiivsemaks jagada kaheks klastriks (K = 2) andmestik,koos the järgmine kõrgeim peak K juures = 5 (täiendavalt Rgure S1). K jaoks = 2, ahpopulations were perseigned kanjaf kaks klastrit koos a rnernbertoipi koefitsient (q) > 0.7. Nagu shown sisse Joonis 2a, hõlmas esimene klaster (nimega S1) MCO ja kõiki ARO populatsioone, samas kui S2 klaster rühmitas kaks TRO populatsiooni. K = 5 korral andmestiku põhjalikuma kirjelduse (joonis 2b), 75% liitumistest määrati ühte viiest klastrist. ARO (S1) ja TRO (S2) eraldamine kinnitati, kuigi mõned ARO populatsioonid segati (q < 0.7, 3) või rühmitati eraldi kahte uude klastrisse S4 ja S7 (vastavalt ARO12 ja ARO5). Huvitav on see, et MCO kaubanduslik tüüp moodustas Apuulia punasest sibulast eraldatud klastri (SXNUMX).
Geneetilised suhted populatsioonide vahel
SSR polümorfism võimaldas koostada geneetilise mitmekesisuse dendrogrammi ja fülogeneetilise analüüsi tulemused on toodud joonisel 3a. Siin jagati iduplasma kollektsioon viieks rühmaks, mida toetasid tugevalt alglaadimisväärtused. ARO7 ja ARO12 populatsioonid eraldati kohe ülejäänud populatsioonidest ja moodustasid kaks erinevat klastrit. Kolmas klaster hõlmas kahte TRO kaubanduslikku populatsiooni, samas kui neljas sõlm jagas MCO üheteistkümnest ARO populatsioonist. Populatsioonide vahel esinevat geneetilist seost uuriti täiendavalt peakoordinaatide analüüsi (PCoA) abil (joonis 3b). Nagu eelnevalt rõhutatud, rühmitati ARO populatsioonid tihedalt, välja arvatud ARO12 ja ARO7, mis ilmusid PCoA graafikul isoleeritud positsioonides. Kaks TRO-d ja MCO populatsioonid olid hajutatud proovitüki alumises paremas paneelis.
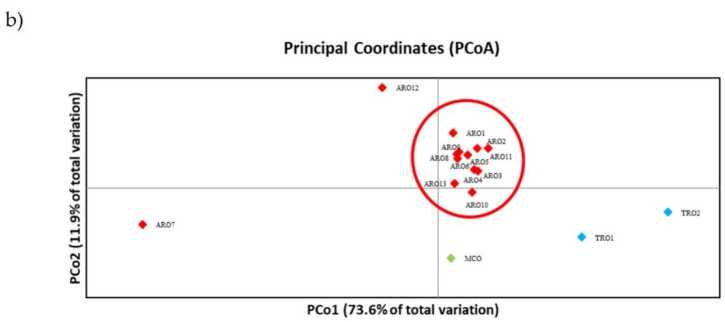
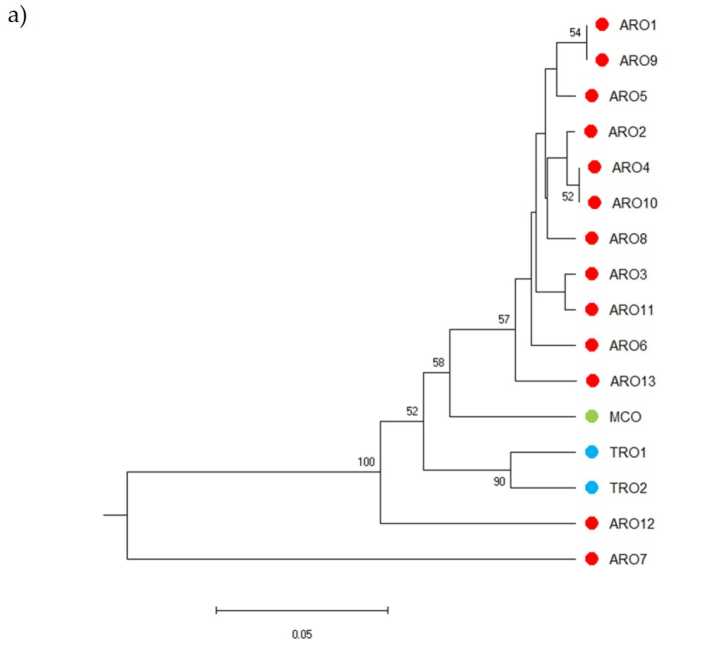
Joonis 3. Geneetiline mitmekesisus 16 A. cepa selles uuringus iseloomustatud populatsioonid nende SSR-profiili põhjal. (a) Geneetilise kauguse UPGMA dendrogramm. Bootstrapi tugiväärtused >50 on näidatud vastavate sõlmede kohal; (b) põhikomponentide analüüs (PCoA). Punase ringiga ümbritsetud klaster ühtis täielikult fülogeneetilise analüüsi abil loodud rühmaga, mille moodustas 11 ARO liitumist.
Arutelu
Lõuna-Itaalias traditsiooniliselt kasvatatavas suures agrobioloogilises mitmekesisuses esindavad sibula maatõud nišitooteid, mida tuleb kaitsta geneetilise erosiooni ohu ja kaasaegsete kultivaridega asendamise ohu eest. Piirkondliku projekti BiodiverSO raames, mille eesmärk on koguda, iseloomustada, edendada ja kaitsta kohaliku pärandiga tugevalt seotud Apuulia piirkonna geneetilisi ressursse, asutasime ARO maatõu 13 populatsioonist koosneva seemnekogu. Teatasime ARO variatsiooni esimesest hinnangust DNA polümorfismide ja kahe biokeemilise parameetri, lahustuva tahke aine ja püroviinamarihappe sisalduse osas, mis on seotud maitseomadustega ja on olulised värskete kuumtöötlemata toodete vastuvõtmisel. Lisaks võrreldi ARO maatõu andmeid kahe teise pigmenteeritud sibula maatõu kohta kogutud andmetega, millega ta sageli eksib.
Biokeemilised analüüsid tõid magusa sibula tööstuse juhiste kohaselt esile 13 ARO populatsiooni magusust, mis on seotud kõrge lahustuva tahke aine sisalduse ja keskmise teravusega. [31]. ARO pirnid olid magusamad kui TRO ja MCO maatõugudel ning neil oli pisut suurem teravus. Kuid sibula magusus tuleneb suhkrusisalduse ja teravuse vahelisest tasakaalust, seetõttu võib see iseloomustus olla kasulik väärtuslike genotüüpide valiku toetamiseks, mida põllumehed teevad tavaliselt ainult morfoloogia põhjal.
Kinnitati, et SSR-markerid on kasulik vahend genotüüpide eristamiseks, kuigi koguti kitsas kasvupiirkonnas, näiteks Acquaviva delle Fonti linnas. Valitud markeritel oli suurem arv alleele kui varem teatatud markeritel [43] ja [44], kuid madalam kui markeritel, millest teatas [45]. Veelgi enam, 50% meie markerite komplektist näitasid PIC-indeksi väärtusi, mis olid suuremad kui 0.5, mis osutus sobivaks kogumis olevate populatsioonide diskrimineerimiseks, nagu soovitas [46]. Populatsioonide mitmekesisuse hindamine näitas Ho ja He vahel sarnaseid väärtusi, mille tulemuseks oli madal Fis väärtused. See on kooskõlas ristuva olemusega A. cepa, kes kannatab tõsiselt sugulusdepressiooni all [47]. Üldine Fis selles uuringus vaadeldud sibulapopulatsioonides arvutatud väärtus (0.054) oli madalam kui varem teatatud väärtus. [45] (0.22) ja peaaegu identne poolt leitud [31] (0.08) ja [48] (0.00, XNUMX), kes hindasid vastavalt Loode-Hispaania ja Nigeri sibula maatõugude geneetilist mitmekesisust. Märkimisväärne heterosügootsuse tase ARO populatsioonides kinnitab arusaama, et Apuulia esindab paljude aiandusliikide mitmekesisuse keskust [32, 42, 49-üks].
AMOVA rõhutas, et enamik selles uuringus genotüübitud kollektsiooni molekulaarseid variatsioone peitub populatsioonides. Siiski on populatsioonide oluline geneetiline diferentseerumine (FPT väärtused) näitasid geneetilise kihistumise esinemist. Tegelikult, kuigi meie tulemused näitasid geneetilise ühtluse olemasolu enamikus ARO populatsioonides, moodustades täpselt määratletud klastri, näitasid ARO7 ja ARO12 populatsioonid selgelt eristatavat geneetilist profiili. Selle tulemuse põhjuseks võib olla nende seemnete erinev päritolu, mida kasutasid kaks põllumajandustootjat, kellelt populatsioonid koguti. Veelgi enam, saadud tulemuste põhjal võib ARO maatõugu pidada geneetilisel tasandil selgelt eristatavaks TRO ja MCO maatõugudest. Hiljutises uuringus [29] hindas mitme Itaalia sibulamaatõu, sealhulgas "Acquaviva", "Tropea" ja "Montoro" geneetilist mitmekesisust. Kuigi autorid kasutasid SNP markereid laiema sibulakollektsiooni geneetilise mitmekesisuse hindamiseks, ei suutnud genotüpiseerimine eristada "Acquavivat" "Tropea" ja "Montoro" sibulatest. Tõenäoliselt on see lahknevus tingitud madalast leitud keskmisest PIC väärtusest (0.292, XNUMX), mis viitab analüüsitavate lookuste tagasihoidlikule üldisele informatiivsusele, nagu väitis [29]. Veelgi enam, selleks, et uurida alamstruktuuri olemasolu nende Itaalia klastris, oleks olnud parem analüüsida Itaalia genotüüpe ülejäänud kollektsioonist eraldi. Tõenäoliselt oleks see võimaldanud visualiseerida geneetilise mitmekesisuse mustrit, mis on seotud geograafilise kihistumise või empiirilise valiku tunnustega.
Kokkuvõtteks võib öelda, et käesolev uuring kujutab endast kõikehõlmavat aruannet kohaliku kultuuripärandiga seotud ja põllumajandustootjate jaoks majandusliku tähtsusega sibula maatõu kohta. Meie tulemused näitavad, et mõne erandiga iseloomustab ARO-d täpselt määratletud geenivaramu, mis väärib säilitamist geneetilise erosiooni ohu eest. Seetõttu on selle väärtusliku geneetilise mitmekesisuse allika esindusliku kollektsiooni loomine olnud ülioluline. Lõpuks võib ARO geneetiline ja fenotüübiline iseloomustus olla kasulik Euroopa Liidu kvaliteedimärkide saamiseks.
Materjalid ja meetodid
Germplasmi kogumine, taimne materjal ja DNA ekstraheerimine
Apuulia piirkonna projekti (BiodiverSO:) raames hangiti 13 ARO maatõu populatsioonist koosnev komplekt. https://www.biodiversitapuglia.it/)Itaalias Bari provintsis asuvas Apuulia väikelinnas Acquaviva delle Fonti missioonide seeria kaudu. Iga liitumise kogumiskohad kaardistati geograafilise teabesüsteemi (GIS) kaudu ja esitati tabelis 4. Lisaks kaasati käesolevasse uuringusse kaks populatsiooni TRO maatõust ja üks populatsioon MCO maatõust ja neid kasutati viidetena. Kogu taimne materjal kasvatati samades keskkonnatingimustes Bari ülikooli katsefarmis “P Martucci” (41° 1'22.08″ N, 16°54'25.95″ E) kaitsepuuris, et vältida risttolmlemist populatsioonisisene tolmeldamine kärbeste abil (Lucilia caesar). 16 populatsiooni iseloomustati sibulate suuruse ja kuju ning naha ja viljaliha värviga seotud tunnuste järgi (tabel S1). Lisaks viidi läbi tahke lahustuva sisalduse analüüs käeshoitava refraktomeetriga ja sibulamahla proovides mõõdeti teravust, lisades 2,4-dinitrofenüülhüdrasiini (0.125%). v/v 2N HCl-s) ja neeldumise hindamine 420 nm juures, nagu on teatanud [31]. Oluliste erinevuste olemasolu kindlakstegemiseks viidi läbi Duncani mitme vahemiku test ja SNK test.
Tabel 4. Selles uuringus kogutud ja genotüpiseeritud populatsioonide loend. Iga populatsiooni kohta esitatakse identifitseerimiskood, kohalik nimi, GPS-koordinaat ja seemneid säilitav geenivaramu.
| kood | Nimi | GPS-koordinaadid | Geenivaramu y |
| ARO1 | Cipolla rossa di Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rossa di Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rossa di Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rossa di Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rossa di Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rossa di Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rossa di Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rossa di Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rossa di Acquaviva | 40°54"51.372 tolli N 16°49"3.504" E | Di.SSPA |
| ARO10 | Cipolla rossa di Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rossa di Acquaviva | 40°52"49.8 tolli N 16°49"48.575" E | Di.SSPA |
| ARO12 | Cipolla rossa di Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rossa di Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa lunga di Tropea | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda di Tropea | - | Di.SSPA |
| MCO | Cipolla ramata di Montoro | - | Di.SSPA |
| y Di.SSPA, Bari ülikooli mulla-, taime- ja toiduteaduste osakond. |
Iga populatsiooni kohta võeti 20 genotüübi lehematerjali proovid ja neid säilitati kuni kasutamiseni temperatuuril -80 °C. Polüsahhariidirikaste liikide puhul, nagu A. cepa, Polüsahhariidi eemaldamise esimesed sammud on kvaliteetse DNA saamiseks hädavajalikud, seetõttu viidi esmased pesud STE puhvris (0.25 M sahharoosi, 0.03 M Tris, 0.05 M EDTA) läbi vastavalt artiklile. [52]. Kogu DNA ekstraheeriti CTAB meetodil [53] ja lõpuks kontrolliti selle kvaliteeti ja kontsentratsiooni Nano Drop 2000 UV-vis spektrofotomeetriga (ThermoScientific, Waltham, MA, USA) ja 0.8% agaroosgeelelektroforeesiga.
SSR-i analüüs
16 EST-SSR praimeri kombinatsiooni, mille on välja töötanud [54] ja varem testitud geneetilise mitmekesisuse uuringutes [43] ja [44] ja 21 genoomilist SSR-i [45-üks] sõeluti, et hinnata nende sobivust (täiendav tabel S4). Genotüpiseerimine viidi läbi ökonoomse fluorestseeruva märgistamise meetodi abil, mille puhul M13 saba lisati igale SSR-praimerile. [56]. PCR segud valmistati 20 gl reaktsioonis, mis sisaldas: 50 ng kogu DNA-d, 0.2 mM dNTP segu, 1X PCR reaktsioonipuhvrit, 0.8 U DreamTaq DNA polümeraasi (Thermo Scientific, Waltham, MA, USA), 0.16 gM pöördpraimerit. , 0.032 gM päripraimerit, mis on pikendatud M13 järjestusega (5'-TGTAAAACGACGGCCAGT-3') ja 0.08 gM universaalset M13 praimerit, mis on märgistatud FAM või NED fluorestsentsvärvidega (Sigma-Aldrich, St. Louis, MO, USA). PCR reaktsioonid viidi läbi SimpliAmp (Applied Biosystems, CA, USA) termotsükleris järgmiste tingimustega enamiku praimeripaaride puhul: 94 °C 5 minutit, 40 tsüklit 94 °C juures 30 sekundit, 58 °C 45 sekundit ja 72 °C 45 sekundit ning lõplik pikenemine 72 °C juures 5 minutit. Nagu ACM446 ja ACM449 puhul, rakendati maandumis-PCR-i, lõõmutades 60 ° C kuni 55 ° C 10 tsükli jooksul, 30 tsüklit temperatuuril 55 ° C, millele järgnes viimane pikendus 5 minutit temperatuuril 72 ° C. PCR tooted laaditi 96-augulisele plaadile ja segati 14 gl Hi-Di Formamide (Life Technologies, Carlsbad, CA, USA) ja 0.5 gL GeneScan 500 ROX Size Standardiga (Life Technologies, Carlsbad, CA, USA). Amplikonid lahutati kapillaaride sekveneerimismasina ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Carlsbad, CA, USA) abil, kus alleelid hinnati kaasdomineerivateks ja määrati, kasutades GeneMapperi tarkvara versiooni 3.7.
Tarkvara GenAlEx 6.5 [57] ja Cervus 3.0.7 [58] kasutati alleelide arvu (Na), efektiivsete alleelide (Ne), täheldatud heterosügootsuse (Ho), eeldatava heterosügootsuse (He), polümorfse teabesisalduse (PIC), Shannoni teabeindeksi (I) ja fikseerimisindeksi (Fis) hindamiseks. ) iga SSR-lookuse jaoks.
Geneetilise mitmekesisuse hindamine
GenAlEx 6.5 hindas geneetilise variatsiooni hierarhilist jaotust sibulapopulatsioonide vahel ja sees [57] molekulaarse dispersiooni analüüsi (AMOVA) abil 999 alglaadimisega, et testida olulisust. Lisaks kasutati GenAlEx 6.5 tarkvara iga populatsiooni mitmekesisuse hindamiseks, arvutades kõigi SSR lookuste Ho, He ja Fis keskmise.
Populatsiooni struktuur tuletati tarkvaras STRUCTURE v.2.3.4 rakendatud Bayesi mudelipõhise klasterdamisalgoritmi abil [59]. Andmekogumit käitati mitme hüpoteetilise klastriga (K), vahemikus 1 kuni 10, määrates iga K väärtuse kohta kümme sõltumatut käitamist. Iga katse puhul viidi tulemuste järjepidevuse kontrollimiseks läbi 100,000 100,000 esialgset sissepõlemisperioodi ja XNUMX XNUMX Markovi ahela Monte Carlo (MCMC) iteratsiooni segude mudeli ja sõltumatute alleelide sageduste alusel populatsioonide vahel. Kõige tõenäolisem K väärtus määrati AK meetodi rakendamisel, mida kirjeldas [60], veebipõhises programmis STRUCTURE HARVESTER [61]. Üksikpopulatsioon määrati konkreetsesse klastrisse, kui selle liikmelisuse koefitsient (q-väärtus) oli suurem kui 0.7, XNUMX, vastasel juhul peeti seda segatud esivanemateks.
Peamine koordinaatide analüüs viidi läbi selleks, et visualiseerida liitumiste vahelisi geneetilisi seoseid, mis ilmnesid Nei geneetilise kauguse maatriksiga (täiendav tabel S5). Alleelisageduste põhjal koostati geneetilise kauguse dendrogramm, rakendades POPTREEW tarkvaras kaalumata paarirühma meetodit aritmeetiliste keskmiste (UPGMA) klasteranalüüsiga. [62]. Hierarhilise klastrite usaldusväärsuse hindamiseks rakendati alglaadimist, määrates andmekogumi 100 uuesti valimi. Lõpuks MEGA X tarkvara [63] kasutati puu joonistamise tarkvarana.
Täiendavad materjalid: Järgnevad on saadaval veebis aadressil http://www.mdpi.com/2223-7747/9/2/260/s1. Tabel S1: ARO-, MCO- ja TRO-pirnide morfoloogiline iseloomustus. Tabel S2: ARO maatõugude ning TRO ja MCO maatõugude jaoks arvutatud heterosügootsuse ja fikseerimise indeksid. Tabel S3: Fpt parameetri paaripõhised väärtused. Tabel S4: uuringus kasutatud SSR-ide loend. Tabel S5. Nei geneetilise kauguse paaripõhine populatsioonimaatriks. Joonis S1: Evanno Delta K-ga muutuvate K väärtuste joondiagramm.
Autori panused: CL ja LR kavandasid uuringu ja kavandasid katse; CL ja PI viisid läbi molekulaarse markerite analüüsi; ARM ja VZ viisid läbi välikatsed; Andmeanalüüsis osalesid RM, SP, GR ja CL; RM ja CL kirjutasid käsikirja. Kõik autorid on käsikirja avaldatud versiooni läbi lugenud ja sellega nõustunud.
Rahastamine: Seda tööd rahastati piirkondliku Apuulia projekti „Apuulia köögiviljaliikide bioloogiline mitmekesisus” (Programma di Sviluppo Rurale per la Puglia 2014–2020) raames. Misura 10—Sottomisura 10.2; grant CUP H92C15000270002, Itaalia.
Tänud: Tänusõnad kuuluvad "Azienda Agricola Iannone Anna" ja "Associazione produttori della vera cipolla rossa di Acquaviva" katses kasutatud taimsete materjalide hankimise eest.
Huvide konflikt: Autorid ei kuulu huvide konflikti.
viited
- 1. Stearn, WT Mitu Alliumi liiki on teada? Kew Mag. 1992, 9, 180-182. [CrossRef]
- 2. FAOSTAT. FAO statistika andmebaas. Internetis saadaval: http://www.fao.org/2017 (vaadatud 8. jaanuaril 2019).
- 3. Block, E. Küüslaugu ja sibula keemia. Sci. Olen. 1985, 252, 114-119. [CrossRef]
- 4. Lee, B.; Jung, JH; Kim, HS Punase sibula antioksüdantse aktiivsuse hindamine rottidel. Food Chem. Toksikool. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM; Moon, J.; Chung, JH; Cha, YJ; Shin, MJ Kvertsetiinirikaste sibulakoore ekstraktide mõju arteriaalsele tromboosile rottidel. Food Chem. Toksikool. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O.; Shiojima, Y.; Igarashi, K. Sibulaekstrakti rasvumisvastane toime zucker-diabeetilistel rasvrottidel. Toitained 2012, 4,1518-1526. [CrossRef]
- 7. Akaš, MSH; Rehman, K.; Chen, S. Vürtsitaim Allium cepa: Toidulisand II tüüpi suhkurtõve raviks. Toitumine 2014, 30, 1128-1137. [CrossRef] [PubMed]
- 8. Wang, Y.; Tian, WX; Ma, XF Sibula pärssiv toime (Allium cepa L.) ekstrakt vähirakkude ja adipotsüütide proliferatsiooni kohta rasvhapete süntaasi inhibeerimise kaudu. Aasia Pac. J. Cancer Prev. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW; Hsu, SC; Chueh, FS; Chen, YY; Yang, JS; Lin, JP; Lien, JC; Tsai, CH; Chung, JG kvertsetiin pärsib inimese SAS-i suuvähi rakkude migratsiooni ja invasiooni NF-kappaB ja maatriksi metalloproteinaas-2/-9 signaaliradade pärssimise kaudu. Anticancer Res. 2013, 33, 1941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA; Milner, JA Küüslauk ja sibul: nende vähktõve ennetavad omadused. Vähk Eelm. Res. 2015, 8,181-189. [CrossRef]
- 11. Forte, L.; Torricelli, P.; Boanini, E.; Gazzano, M.; Rubini, K.; Fini, M.; Bigi, A. Kvertsetiiniga funktsionaliseeritud hüdroksüapatiidi antioksüdandid ja luude parandamise omadused: in vitro osteoblastide-osteoklastide-endoteliaalsete rakkude ühiskultuuri uuring. Acta Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y.; Iwasaki, K.; Mikami, M.; Yagihashi, A. Üheteistkümne maitseprekursori, S-Alk(en)üül-L-tsüsteiini derivaatide jaotus seitsmes Alliumi köögiviljas. Food Sci. Technol. Res. 2011, 17, 55-62. [CrossRef]
- 13. Block, E. Perekonna Alliumi väävelorgaaniline keemia – mõju väävli orgaanilisele keemiale. Angew. Chem. Int. Ed. Ingl. 1992, 31, 1135-1178. [CrossRef]
- 14. Griffiths, G.; Trueman, L.; Crowther, T.; Thomas, B.; Smith, B. Sibul – ülemaailmne kasu tervisele. Fütoter. Res. 2002,16, 603-615. [CrossRef]
- 15. Schwimmer, S.; Weston, WJ Püruviinhappe ensümaatiline arendamine sibulas teravuse mõõtmiseks. J. Agric. Toidu keemia. 1961, 9, 301-304. [CrossRef]
- 16. Ketter, KAT; Randle, WM Teravuse hindamine sibulas. sisse Testitud uuringud laboratoorseks õpetamiseks; Karcher, SJ, toim.; Bioloogialaborihariduse assotsiatsioon (ABLE): New York, NY, USA, 1998; 19. köide, lk 177-196.
- 17. Hanelt, P Taksonoomia, evolutsioon ja ajalugu. sisse Onions and Allied Crops, Vol. I. Botaanika, füsioloogia ja geneetika; Rabinowitch, HD, Brewster, JL, toim.; CRC Press: Boca Raton, FL, USA, 1990; lk 1-26.
- 18. Rabinowitch, HD; Currah, L. Allium Crop Science: hiljutised edusammud; CABI kirjastus: Wallingford, Suurbritannia, 2002.
- 19. Mallor, C.; Carravedo, M.; Estopanan, G.; Mallor, F. Sibula geneetiliste ressursside iseloomustus (Allium cepa L.) Hispaania teisest mitmekesisuse keskusest. Span. J. Agric. Res. 2011, 9, 144-155. [CrossRef]
- 20. Ferioli, F.; D'Antuono, LF Fenoolide ja tsüsteiinsulfoksiidide hindamine kohalikus sibula ja šalottsibula iduplasmas Itaaliast ja Ukrainast. Genet. Ressurss. Crop Evol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos, SA; Fernandes, A.; Barros, L.; Ferreira, ICFR; Ntatsi, G. Kreekast pärit sibula kohaliku maatõu 'vatikiotiko' morfoloogiline, toitumisalane ja keemiline kirjeldus. Food Chem. 2015,182, 156-163. [CrossRef]
- 22. Liguori, L.; Adiletta, G.; Nazzaro, F.; Fratianni, F.; Di Matteo, M.; Albanese, D. Vahemere piirkonna erinevate sibulasortide biokeemilised, antioksüdantsed omadused ja antimikroobne toime. J. Food Meas. Iseloom. 2019,13, 1232-1241. [CrossRef]
- 23. Yoo, KS; Pike, L.; Crosby, K.; Jones, R.; Leskovar, D. Erinevused sibula teravuses kultivaride, kasvukeskkonna ja sibulate suuruse tõttu. Sci. Hortic. 2006,110, 144-149. [CrossRef]
- 24. Beesk, N.; Perner, H.; Schwarz, D.; George, E.; Kroh, LW; Rohn, S. Genotüübist mõjutatud kvertsetiin-3, 4'-O-diglükosiidi, kvertsetiin-4'-O-monoglükosiidi ja kvertsetiini jaotus sibula sibula (Allium cepa L.) erinevates osades. Food Chem. 2010,122, 566-571. [CrossRef]
- 25. Caruso, G.; Conti, S.; Villari, G.; Borrelli, C.; Melchionna, G.; Minutolo, M.; Russo, G.; Amalfitano, C. Istutamisaja ja taimede tiheduse mõju sibula saagikusele, kvaliteedile ja antioksüdantide sisaldusele (Allium cepa L.) Lõuna-Itaalias. Sci. Hortic. 2014,166, 111-120. [CrossRef]
- 26. Perez-Gregorio, MR; Regueiro, J.; Simal-Gandara, J.; Rodrigues, AS; Almeida, DPF Sibula lisandväärtuse suurendamine antioksüdantsete flavonoidide allikana: kriitiline ülevaade. Crit. Rev. Food Sci. Nutr. 2014, 541050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Schweiggert, RM; Carle, R. Viljelusmeetodi ja kultivaride valiku mõju sibula lahustuvatele süsivesikutele ja teravatele põhimõtetele (Allium cepa L.). J. Agric. Toidu keemia. 2018, 66, 12827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I.; Carbone, V.; Spagnuolo, C.; Minasi, P.; Russo, GL Kahe Lõuna-Itaalia kultivari flavonoidide identifitseerimine ja kvantifitseerimine Allium cepa L., Tropea (punane sibul) ja Montoro (vasksibul) ning nende võime kaitsta inimese erütrotsüüte oksüdatiivse stressi eest. J. Agric. Toidu keemia. 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Esposito, S.; Carucci, F.; Frusciante, L.; Carputo, D.; Aversano, R. Sibula suure läbilaskevõimega genotüpiseerimine näitab geneetilise mitmekesisuse struktuuri ja informatiivseid SNP-sid, mis on kasulikud molekulaarseks aretuseks. Mol. Tõug. 2019, 39, 5. [CrossRef]
- 30. Mercati, F.; Longo, C.; Poma, D.; Araniti, F.; Lupini, A.; Mammano, MM; Fiore, MC; Abenavoli, MR; Sunseri, F Itaalia pika säilivusajaga tomati geneetiline variatsioon (Solanum lycopersicum L.) kogumine SSR-i ja morfoloogiliste viljatunnuste abil. Genet. Ressurss. Crop Evol. 2014, 62, 721-732. [CrossRef]
- 31. Gonzalez-Perez, S.; Mallor, C.; Garces-Claver, A.; Merino, F.; Taboada, A.; Rivera, A.; Pomar, F.; Perovic, D.; Silvar, C. Geneetilise mitmekesisuse ja kvaliteediomaduste uurimine sibulakollektsioonis (Allium cepa L.) Loode-Hispaania maatõugud. Geneetika 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Iovieno, P.; Centomani, I.; Marcotrigiano, AR; Fanelli, V.; Mimiola, G.; Summo, C.; Pavan, S.; Ricciardi, L. Kapsa geneetiline, bioagronoomiline ja toitumisalane iseloomustus (Brassica oleracea L. var. acephala) mitmekesisus Lõuna-Itaalias Apuulias. mitmekesisus 2018,10, 25. [CrossRef]
- 33. Bardaro, N.; Marcotrigiano, AR; Bracuto, V.; Mazzeo, R.; Ricciardi, F.; Lotti, C.; Pavan, S.; Ricciardi, L. Resistentsuse geneetiline analüüs Orobanche crenata (Forsk.) hernes (Pisum sativum L.) madala strigolaktooniga liin. J. Plant Pathol. 2016, 98 671-675.
- 34. Wako, T.; Tsukazaki, H.; Yaguchi, S.; Yamashita, K.; Ito, S.; Shigyo, M. Kvantitatiivsete tunnuste lookuste kaardistamine sibula kokkupanemise aja jaoks (Allium fistulosum L.). Euphytica 2016, 209, 537-546. [CrossRef]
- 35. Dhaka, N.; Mukhopadhyay, A.; Paritosh, K.; Gupta, V.; Pental, D.; Pradhan, AK Geensete SSR-ide tuvastamine ja SSR-põhise sidekaardi koostamine Brassica juncea. Euphytica 2017, 213, 15. [CrossRef]
- 36. Anandhan, S.; Mote, SR; Gopal, J. Sibulasordiidentiteedi hindamine SSR-markerite abil. Seed Sci. Technol. 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K.; Svoboda, P.; Ovesna, J. Tšehhist pärit sibulakultuuride eristamiseks mõeldud markerite komplekti valimine ja valideerimine. Tšehhi J. Genet. Taimetõug. 2015, 51, 62-67. [CrossRef]
- 38. Di Rienzo, V.; Miazzi, MM; Fanelli, V.; Sabetta, W.; Montemurro, C. Apuulia oliiviõli iduplasma bioloogilise mitmekesisuse säilitamine ja iseloomustamine. Acta Hortic. 2018,11991-6. [CrossRef]
- 39. Mallor, C.; Arnedo-Andres, A.; Garces-Claver, A. Hispaania keele geneetilise mitmekesisuse hindamine Allium cepa maatõugud sibulakasvatuseks, kasutades mikrosatelliitmarkereid. Sci. Hortic. 2014,170, 24-31. [CrossRef]
- 40. Rivera, A.; Mallor, C.; Garces-Claver, A.; Garcia-Ulloa, A.; Pomar, F.; Silvar, C. Sibula geneetilise mitmekesisuse hindamine (Allium cepa L.) Loode-Hispaania maatõugud ja võrdlus Euroopa variatiivsusega. NZJ Crop Hortic. 2016, 44, 103-120. [CrossRef]
- 41. De Giovanni, C.; Pavan, S.; Taranto, F.; Di Rienzo, V.; Miazzi, MM; Marcotrigiano, AR; Mangini, G.; Montemurro, C.; Ricciardi, L.; Lotti, C. Kikerherne globaalse iduplasma kollektsiooni geneetiline variatsioon (Cicer arietinum L.), sealhulgas Itaalia liitumised, millel on geneetilise erosiooni oht. Physiol. Mol. Biol. Taimed 2017, 23, 197-205. [CrossRef]
- 42. Mazzeo, R.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Pavan, S.; Ricciardi, L.; Lotti, C. Geneetiline mitmekesisus brokkoli rabes (Brassica rapa L. subsp. sylvestris (L.) Janch.) Lõuna-Itaaliast. Sci. Hortic. 2019, 253, 140-146. [CrossRef]
- 43. Jakse, M.; Martin, W.; McCallum, J.; Havey, M. Ühe nukleotiidi polümorfismid, indelid ja lihtsad järjestuse kordused sibulasordi identifitseerimiseks. J. Am. Soc. Hortic. Sci. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Geneetilise mitmekesisuse analüüs ja ühe nukleotiidi polümorfismi markerite arendamine kultiveeritud sibulas, mis põhineb ekspresseeritud järjestuse märgise-lihtsate järjestuste kordusmarkeritel. J. Am. Soc. Hortic. Sci. 2008,133, 810-818. [CrossRef]
- 45. Baldwin, S.; Pither-Joyce, M.; Wright, K.; Chen, L.; McCallum, J. Tugevate genoomsete lihtsate järjestuste kordusmarkerite väljatöötamine sibula sees ja hulgas geneetilise mitmekesisuse hindamiseks (Allium cepa L.) populatsioonid. Mol. Tõug. 2012, 30, 1401-1411. [CrossRef]
- 46. DeWoody, JA; Honeycutt, RL; Skow, LC Microsatellite markerid valgesabalises hirves. J. Hered. 1995, 86 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M.; Hassanpanah, D. Iraani sibul (Allium cepa L.) kultivarid reageerivad sugulusdepressioonile. Maailma rakendus. Sci. J. 2010,11, 426-428.
- 48. Abdou, R.; Bakasso, Y.; Saadou, M.; Baudoin, JP; Hardy, OJ Nigeri sibulate geneetiline mitmekesisus (Allium cepa L.), mida hinnatakse lihtsa järjestuse kordusmarkeritega (SSR). Acta Hortic. 2016,1143 77-90. [CrossRef]
- 49. Pavan, S.; Lotti, C.; Marcotrigiano, AR; Mazzeo, R.; Bardaro, N.; Bracuto, V.; Ricciardi, F.; Taranto, F.; D'Agostino, N.; Schiavulli, A.; et al. Erinev geneetiline klaster kultiveeritud kikerhernes, mis ilmneb genoomi hõlmava markerite avastamise ja genotüpiseerimisega. Taime genoom 2017, 201710. [CrossRef]
- 50. Pavan, S.; Marcotrigiano, AR; Ciani, E.; Mazzeo, R.; Zonno, V.; Ruggieri, V.; Lotti, C.; Ricciardi, L. Meloni genotüpiseerimine järjestuse järgi (Cucumis melo L.) iduplasma kogumine sekundaarsest mitmekesisuse keskusest toob esile erinevate geenifondide geneetilise variatsiooni mustrid ja genoomilised omadused. BMC Genom. 2017, 18, 59. [CrossRef]
- 51. Di Rienzo, V.; Sion, S.; Taranto, F.; D'Agostino, N.; Montemurro, C.; Fanelli, V.; Sabetta, W.; Boucheffa, S.; Tamendjari, A.; Pasqualone, A.; et al. Vahemere basseini oliivipopulatsiooni geneetiline voog. Eakaaslane J. 2018, 6. [CrossRef]
- 52. Karjane, LD; McLay, TG Kaks mikroskaala protokolli DNA eraldamiseks polüsahhariidirikkast taimekoest. J. Plant Res. 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Taime DNA eraldamine värskest koest. Keskenduma 1990,12, 13-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Martin, W.; Zewdie, Y.; McCallum, J.; Catanach, A.; Rutherford, P.; Valamu, KC; Jenderek, M.; et al. Ainulaadne 11,008 XNUMX sibula ekspresseeritud järjestusmärgise komplekt paljastab ekspresseeritud järjestuse ja genoomilised erinevused üheiduleheliste seltside sparglite ja poales vahel. Taimerakk 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, HR; Hyun, JY; Laul, KH; Kim, KH; Kim, JE; Hur, CG; Harn, CH Markeri väljatöötamine sibula geneetilise puhtuse testimiseks SSR Finderi abil. Korea J. Tõug. Sci. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Majanduslik meetod PCR fragmentide fluorestsentsmärgistamiseks. Nat. Biotehnoloogia. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R.; Smouse, PE GenAlEx 6.5: geneetiline analüüs Excelis. Rahvastiku geneetiline tarkvara õpetamiseks ja teadustööks: värskendus. Bioinformaatika 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski, ST; Koonus, ML; Marshall, TC Arvutiprogrammi CERVUS genotüpiseerimisvigade arvestamise ülevaatamine suurendab edu isaduse määramisel. Mol. Ecol. 2007,16, 1099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M.; Rosenberg, NA; Donnelly, P. Assotsiatsiooni kaardistamine struktureeritud populatsioonides. Olen. J. Hum. Genet. 2000, 67 170-181. [CrossRef]
- 60. Evanno, G.; Regnaut, S.; Goudet, J. Indiviidide klastrite arvu tuvastamine tarkvara abil STRUKTUUR: simulatsiooniuuring. Mol. Ecol. 2005,14, 2611-2620. [CrossRef]
- 61. Earl, D.; VonHoldt, B. STRUKTUURI HARVESTER: veebisait ja programm STRUKTUURI väljundi visualiseerimiseks ja Evanno meetodi rakendamiseks. Konserveerida. Genet. Ressurss. 2011, 4. [CrossRef]
- 62. Takezaki, N.; Nei, M.; Tamura, K. POPTREEW: POPTREE veebiversioon alleelisageduse andmetest populatsioonipuude koostamiseks ja mõne muu suuruse arvutamiseks. Mol. Biol. Evol. 2014, 31 1622-1624. [CrossRef]
- 63. Kumar, S.; Stecher, G.; Li, M.; Knyaz, C.; Tamura, K. MEGA X. Molekulaarevolutsiooniline geneetika analüüs arvutiplatvormidel. Mol. Biol. Evol. 2018, 35, 1547-1549. [CrossRef]